Western blot(蛋白印跡)作為科研研究中最為平常的實(shí)驗(yàn),卻蘊(yùn)含了很多知識(shí),可謂是小實(shí)驗(yàn)里卻有大文章。盡管絕大多數(shù)研究僧在接觸該實(shí)驗(yàn)時(shí)都會(huì)被虐的體無完膚,卻也在和WB斗志斗勇的過程中積累了不少經(jīng)驗(yàn)。正所謂前人種樹,后人乘涼,現(xiàn)在小魚就把各位前輩做WB的各種經(jīng)驗(yàn)總結(jié)起來,希望對(duì)大家能有所幫助。
WB的基本原理
在電場(chǎng)的作用下將電泳分離的多肽從聚丙烯酰胺凝膠轉(zhuǎn)移至一種固相支持體,然后用這種多肽的特異抗體來檢測(cè),經(jīng)常用于目的蛋白的表達(dá)特性分析、組織定位、表達(dá)量分析及與其他蛋白的互作。依其原理,可分為兩種方法:A、直接法和B、間接法。
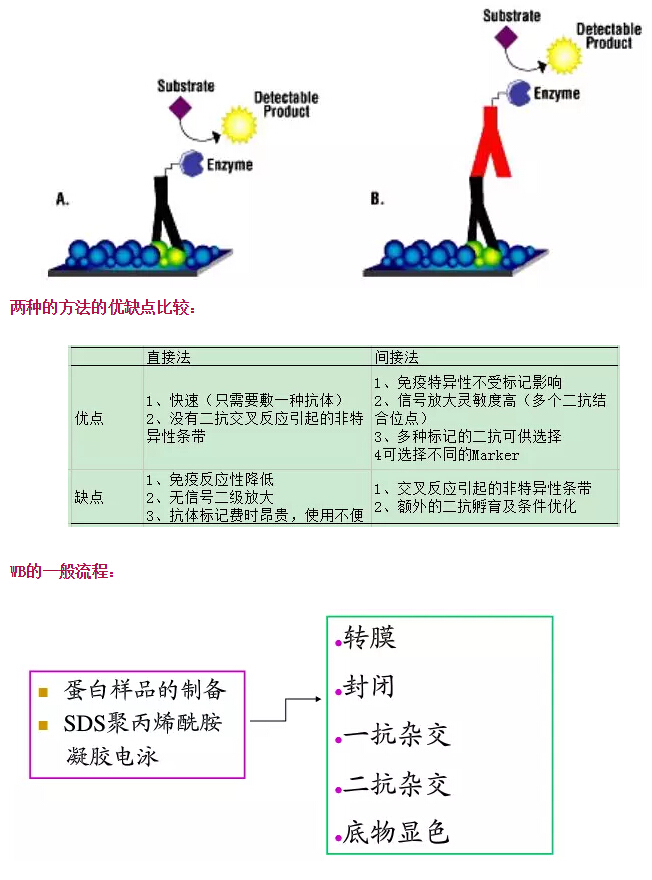
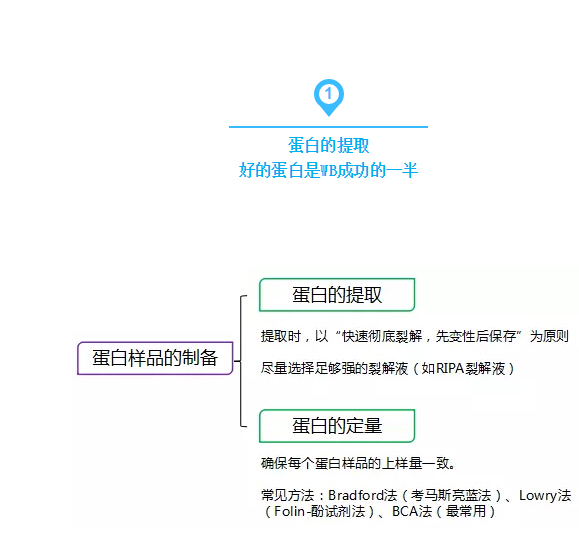
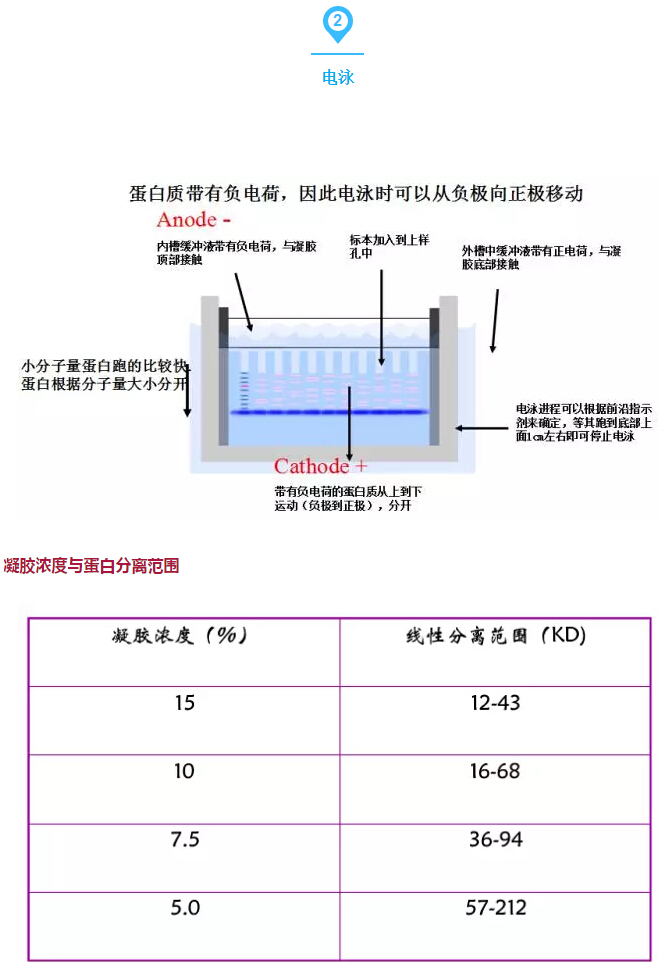
經(jīng)驗(yàn)總結(jié):
1:合適的鹽濃度下,保持蛋白質(zhì)的最大溶解性和可重復(fù)性。
2:盡量除去核酸,多糖,脂類等干擾分子
3:提取蛋白質(zhì)過程中,應(yīng)在低溫環(huán)境下進(jìn)行,以抑制蛋白酶的水解作用(可加入適合的蛋白酶抑制劑)。
4:蛋白樣品建議分裝后冷凍干燥或直接以液體態(tài)置-80℃中保存,不要反復(fù)凍融。
5:蛋白濃度低時(shí),可使用超濾膜濃縮或者用真空凍干機(jī)將蛋白凍干。

經(jīng)驗(yàn)總結(jié):
1:上樣時(shí):根據(jù)蛋白表達(dá)豐度調(diào)整蛋白上樣量,盡量保證每孔上樣量保持一致。
2:膠最好現(xiàn)配現(xiàn)用,如果需要保存,最好用濕潤(rùn)的保鮮膜包好并置于4℃冰箱中。
3:為了檢測(cè)整個(gè)實(shí)驗(yàn)系統(tǒng)或校準(zhǔn)實(shí)驗(yàn)結(jié)果,需要設(shè)置內(nèi)參(一般指由管家基因編碼表達(dá)的蛋白)。

4:為了確保western blot結(jié)果的準(zhǔn)確性和特異性,設(shè)置合適正確的對(duì)照是必不可少,一般需要設(shè)置的對(duì)照如下——
陽(yáng)性對(duì)照:明確表達(dá)檢測(cè)蛋白的組織或細(xì)胞,用于檢測(cè)抗體的工作效率;
陰性對(duì)照:明確不表達(dá)檢測(cè)蛋白組織或細(xì)胞,用于檢測(cè)抗體的特異性;
二抗對(duì)照:不加一抗,用于檢測(cè)二抗的特異性;
內(nèi)參對(duì)照:檢測(cè)標(biāo)本的質(zhì)量和二抗系統(tǒng)
空白對(duì)照:不加一抗和二抗;用于檢測(cè)膜的性質(zhì)和封閉的效果。

用于western blot的雜交膜主要有兩種:NC膜和PVDF膜,可依據(jù)目的蛋白與膜的結(jié)合能力及膜的孔徑來挑選不同的轉(zhuǎn)移膜。
兩個(gè)膜之間的比較:
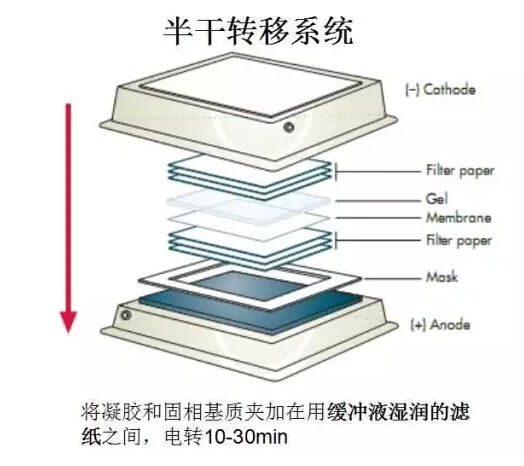
轉(zhuǎn)膜方法:分為兩種濕轉(zhuǎn)法和半干法
經(jīng)驗(yàn)總結(jié):
1:膠在負(fù)極,膜靠近正極;濾紙不要大過膜,防止短路;
2:夾好膜和凝膠后,確定在凝膠、膜和濾紙之間沒有氣泡存在,否則會(huì)導(dǎo)致轉(zhuǎn)膜不完全。
3:注意一定要戴手套或塑料鑷子接觸膜,避免手上的蛋白和油脂降低轉(zhuǎn)膜效率。
4:轉(zhuǎn)膜過程中,尤其是高電流快速轉(zhuǎn)膜時(shí),通常 會(huì)有非常嚴(yán)重的發(fā)熱現(xiàn)象,最好把轉(zhuǎn)膜槽放置在冰浴中進(jìn)行轉(zhuǎn)膜。
5:對(duì)于濕轉(zhuǎn)法:一般轉(zhuǎn)膜的電流在200mA-400mA之間,轉(zhuǎn)膜時(shí)間為30-60分鐘。也可以在15-20mA轉(zhuǎn)膜過夜。大片段的>50KD的可以選用350mA,小片段的可以用250mA。具體的轉(zhuǎn)膜時(shí)間要根據(jù)目的蛋白的大小而定,目的蛋白的分子量越大,需要的轉(zhuǎn)膜時(shí)間越長(zhǎng),目的蛋白的分子量越小,需要的轉(zhuǎn)膜時(shí)間越短。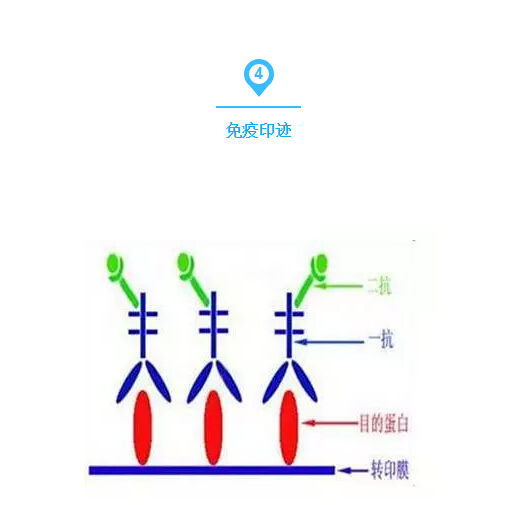
經(jīng)驗(yàn)總結(jié):
1:常見的封閉液有5%脫脂奶粉、BSA和Western Blot膜封閉液(生物試劑公司提供)。但是封閉液的選取具體得看抗體說明書,有的抗體是明確要求只能用BSA,而封閉液濃度的選擇也是具體得看抗體的要求,但是一般情況5%BSA會(huì)比5%牛奶的效果好。
2:選擇抗體時(shí),一方面需要考慮所選抗體是否能識(shí)別凝膠電泳后轉(zhuǎn)印至膜上的變性蛋白,另一方面需要考慮所選抗體是否會(huì)引起交叉反應(yīng)條帶。

WB做完后,有時(shí)需要對(duì)結(jié)果進(jìn)行定量。然而最備受推崇的定量分析軟件Quantiy One軟件因其高昂的售價(jià)令很多人望而卻步,但除了該軟件外還有一個(gè)比較簡(jiǎn)單的圖像處理軟件ImageJ可以很方便的進(jìn)行灰度和密度分析。
ImageJ的軟件界面
1.ImageJ對(duì)WB條帶進(jìn)行灰度分析
1)File|Open打開WB結(jié)果圖片
2)圖片類型設(shè)置:Image|Type|8bit
3)去除圖片背景:Process|Subtract Background
在Subtract Background窗口按照以下條件進(jìn)行設(shè)置:
4)設(shè)置定量參數(shù):Analyze |SetMeasurements,點(diǎn)擊Area,Mean Gray Value及Integrated Density
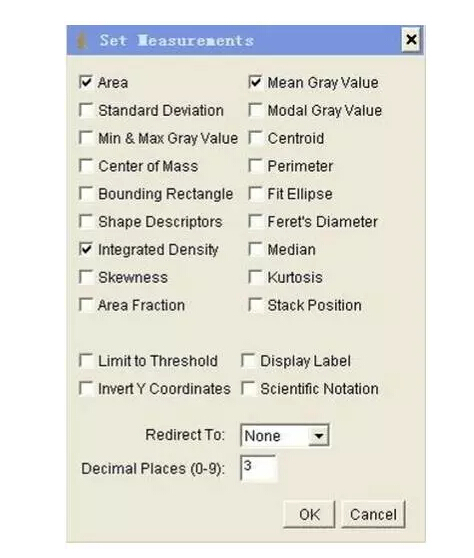
5)設(shè)置單位: Analyze|SetScale,在“unit of length”的方框里輸入“pixels”
6)將圖片轉(zhuǎn)換成亮帶,Edit|Invert

7)選擇Freehand Selection,盡量把條帶圈起來,點(diǎn)擊鍵盤m,出來IntDen灰度值
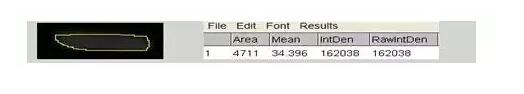
8)復(fù)制數(shù)據(jù)IntDen進(jìn)行分析
2. Image J 對(duì)WB條帶進(jìn)行密度分析
1)步驟同前,F(xiàn)ile|Open打開WB結(jié)果圖片
2)如果條帶不正,需修正

Image transform rotate調(diào)節(jié)angle值,直到條帶水平為止
3)選中矩形選項(xiàng),圈中第一個(gè)條帶,AnalyzeGels Select Firstlane(快捷鍵Ctrl +1),然后移動(dòng)第一個(gè)條帶上的矩形到第二個(gè)條帶上,Analyze Gels Select Second Lane(快捷鍵Ctrl+2),最后Analyze GelPlotlanes
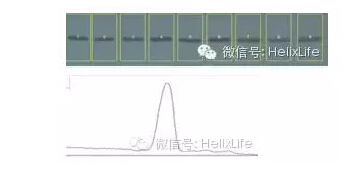
選中直線工具,將開口的波峰關(guān)閉

選中魔棒工具,點(diǎn)擊波峰可以顯示波峰下面積,即條帶的密度值

以第一個(gè)數(shù)值為基數(shù),其他數(shù)值與第一個(gè)數(shù)值的比值即為相對(duì)密度。

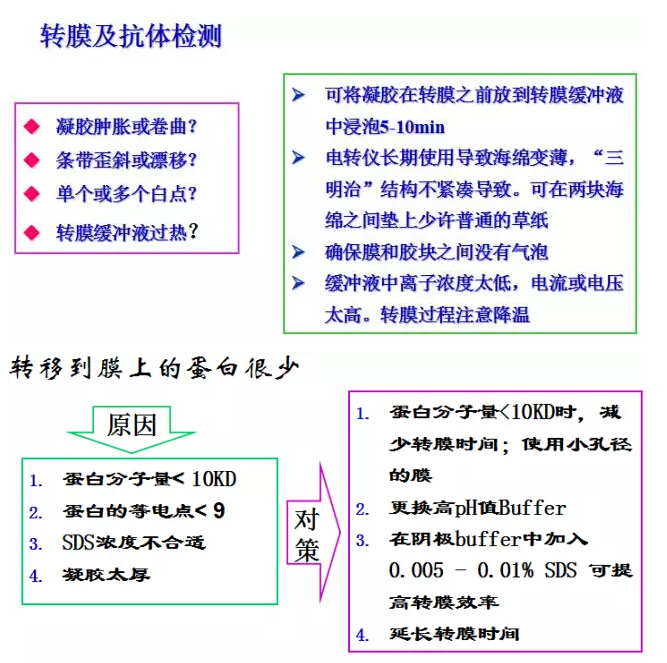
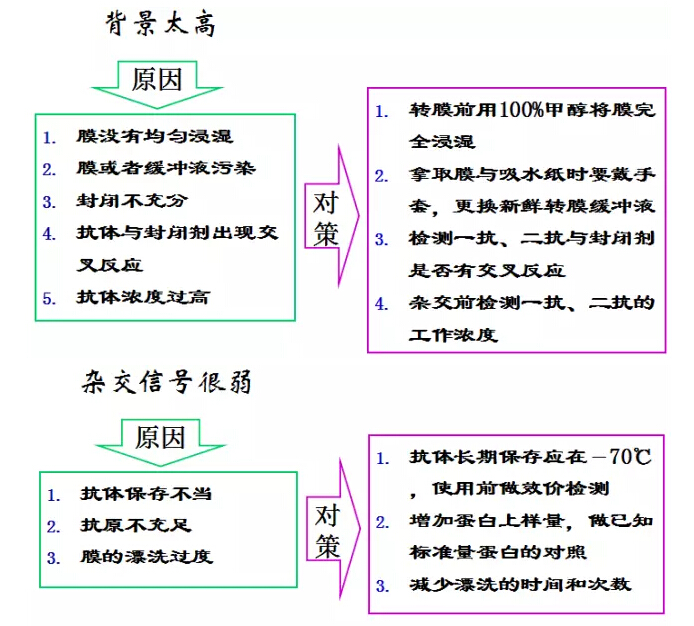
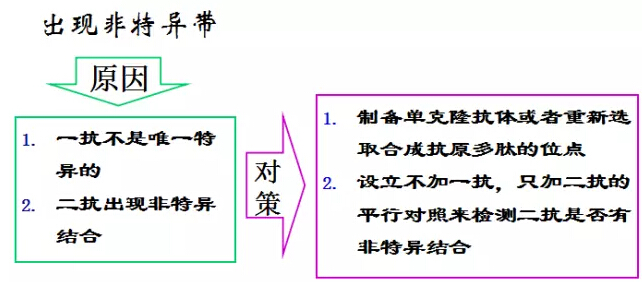
另附前輩們11條“濟(jì)世”經(jīng)驗(yàn)

1、抽提出某個(gè)蛋白第一次檢測(cè),因?yàn)椴恢辣磉_(dá)量咋樣,可以減少裂解液(這樣蛋白濃度高一些),上樣量加大,抗體濃度大一點(diǎn),增加出結(jié)果的幾率,否則出不來結(jié)果不知道是因?yàn)榈鞍琢刻∵€是抗體等其他條件影響,有結(jié)果后再根據(jù)條帶的亮度調(diào)整各種試劑的用量。
2、同時(shí)檢測(cè)兩種蛋白或兩個(gè)樣本的同種蛋白時(shí),蛋白抽提出來后測(cè)濃度,調(diào)整每個(gè)孔的蛋白上樣量一致,通常做法時(shí),做標(biāo)準(zhǔn)曲線,再計(jì)算待測(cè)蛋白的濃度,下面是偷懶的辦法:直接用酶標(biāo)儀測(cè)這兩個(gè)樣品的吸光度,根據(jù)吸光度值將兩個(gè)樣品的蛋白濃度調(diào)整成一致后上樣。吸光度跟蛋白濃度成正比,沒必要一定要測(cè)量出具體濃度,而且只要使我研究的一對(duì)蛋白濃度調(diào)整一樣(對(duì)照組,處理組),沒必要將不同樣本的各組均調(diào)節(jié)成一個(gè)濃度。(懶人有懶人的活法,但是我懶得有原則)
3、科研小白注意黑膠白膜,黑膠白膜,黑膠白膜,重要的事情說三遍。轉(zhuǎn)膜是最好是將膜放在下面,膠放上面,否則會(huì)有鏡像效果,等轉(zhuǎn)完膜后拿出膜時(shí),把膜反過來時(shí),上樣順序會(huì)左右顛倒,因?yàn)槟z無正反,膜有正反。
4、marker盡量不要放在中間,放在兩邊作為順序的標(biāo)記,或者,在膠剝離出來后和PVDF膜的一角剪掉一小塊作為標(biāo)記。(翻過來翻過去,咦,記不得哪邊是哪邊了)
5、封閉的時(shí)間可以延長(zhǎng)問題不大,但是跑膠電泳時(shí)不能將膠長(zhǎng)時(shí)間放在儀器里面,而應(yīng)該放在轉(zhuǎn)膜液里固定(里面有甲醛,可固定蛋白),如果在沒有電流下蛋白一直在膠內(nèi) ,蛋白未被固定,會(huì)擴(kuò)散,轉(zhuǎn)完膜后條帶難看。(甲醛是什么呀,就是大家經(jīng)常報(bào)道的新裝修的房子甲醛超標(biāo),所以實(shí)驗(yàn)狗不容易呀,每天跟這些有毒的東西打交道。)
6、封閉不一定要使用脫脂牛奶,3%BSA也可以,做磷酸化蛋白是盡量使用BSA可以降低背景。一般的實(shí)驗(yàn)還是用便宜的脫脂牛奶。
7、如果一次性需要檢測(cè)多個(gè)蛋白,電泳后可根據(jù)marker(即分子量)將膜剪開,分別不同的抗體孵育,可一次檢測(cè)多個(gè)蛋白;當(dāng)兩個(gè)蛋白分子量很相近PVDF膜無法剪開時(shí),可先曝表達(dá)弱的蛋白,再用抗體洗脫液將已結(jié)合的一抗、二抗洗去,這樣一張印跡膜可以多次使用,再曝表達(dá)強(qiáng)的蛋白,但注意的是此種方法可由于劇烈處理丟失某些表位。
8、買一個(gè)抗體孵育槽可以節(jié)省抗體的使用量,每個(gè)小槽可以孵一張膜。(土豪請(qǐng)忽略這一條,哪里買,問淘寶)

9、內(nèi)參因?yàn)槭褂昧看螅忻嫔嫌袔RP的內(nèi)參出售(言外之意就是一抗上面就帶HRP,就不用孵二抗了),前幾次摸條件時(shí),用帶HRP的內(nèi)參,可以直接一抗后先曝下內(nèi)參,如果內(nèi)參不齊,目的基因暫時(shí)就不用孵育了,等調(diào)節(jié)蛋白上樣量一致后再去檢測(cè)目的基因。
10、抽提蛋白時(shí)全程都要在冰上, 因?yàn)榧恿思?xì)胞裂解液后細(xì)胞被破壞,細(xì)胞內(nèi)的各種酶被釋放,如果不在冰上操作,蛋白容易降解,如果開始抽提蛋白,建議一次性操作到加上loading buffer煮蛋白變性的步驟,煮蛋白的將蛋白變性,后不易降解,如果要長(zhǎng)期保存,放到-20度。
11、頻繁做WB時(shí),可以一次可以多配幾塊電泳膠,running buffer 4度保存,省的每次配膠。
